-
 Tất cả người dân chú ý: Hàng triệu xe máy đối mặt với bộ quy chuẩn nghiêm ngặt từ cuối tháng 6
Tất cả người dân chú ý: Hàng triệu xe máy đối mặt với bộ quy chuẩn nghiêm ngặt từ cuối tháng 6 -
 Đón tín hiệu vui từ xăng E10: Dự báo giảm sâu gần 1.500 đồng/lít và hướng tới cơ chế giá độc lập
Đón tín hiệu vui từ xăng E10: Dự báo giảm sâu gần 1.500 đồng/lít và hướng tới cơ chế giá độc lập -
 Xót xa vụ bé trai 11 tuổi tử vong nghi do mẹ kế bạo hành: Cả xóm ngỡ ngàng vì "chưa từng biết sự tồn tại của em"
Xót xa vụ bé trai 11 tuổi tử vong nghi do mẹ kế bạo hành: Cả xóm ngỡ ngàng vì "chưa từng biết sự tồn tại của em" -
 Dự báo điểm chuẩn lớp 10 tại TP.HCM: Đề "dễ thở", sức nóng cạnh tranh tăng cao
Dự báo điểm chuẩn lớp 10 tại TP.HCM: Đề "dễ thở", sức nóng cạnh tranh tăng cao -
 Người mẹ bế 2 con nhỏ đi bộ dưới nắng nóng, từ chối mọi hỗ trợ đã đồng ý quay về Hải Phòng sau cuộc gặp này
Người mẹ bế 2 con nhỏ đi bộ dưới nắng nóng, từ chối mọi hỗ trợ đã đồng ý quay về Hải Phòng sau cuộc gặp này -
 Cha chết lặng khi con gái báo tin "Bố ơi, mẹ và em cùng anh chị chết đuối rồi": Tiếng khóc của người ở lại
Cha chết lặng khi con gái báo tin "Bố ơi, mẹ và em cùng anh chị chết đuối rồi": Tiếng khóc của người ở lại -
 Vụ nữ du khách kể chuyện "tâm linh" khi du lịch Ninh Bình: Người đăng có thể bị xử lý hình sự?
Vụ nữ du khách kể chuyện "tâm linh" khi du lịch Ninh Bình: Người đăng có thể bị xử lý hình sự? -
 Xe tải lật nghiêng sau cú tông mạnh vào trạm cân, quốc lộ 5 tê liệt nhiều giờ
Xe tải lật nghiêng sau cú tông mạnh vào trạm cân, quốc lộ 5 tê liệt nhiều giờ -
 Hà Nội tạm cấm, hạn chế nhiều tuyến đường trong hai ngày 7-8/6
Hà Nội tạm cấm, hạn chế nhiều tuyến đường trong hai ngày 7-8/6 -
 Vợ Thiếu tá công an hy sinh khi truy bắt "cát tặc" được tuyển dụng vào lực lượng Công an nhân dân
Vợ Thiếu tá công an hy sinh khi truy bắt "cát tặc" được tuyển dụng vào lực lượng Công an nhân dân
Xã hội
21/12/2021 13:46WHO không chấp nhận kit test của Công ty Việt Á: Bộ Y tế nói gì?
Vào khoảng tháng 4 và tháng 5-2020, một số báo chí trong nước đưa tin bộ kit xét nghiệm LightPower iVASARS-CoV-2 1stRT-rPCR Kit được WHO chấp thuận với mã số EUL 0524‐210‐00.
Theo báo cáo công khai về đánh giá sử dụng khẩn cấp của WHO ngày 20-10-2020, kết quả thẩm định là của tổ chức này với bộ xét nghiệm COVID-19 của Việt Á là: Not Accepted - Không được chấp nhận.
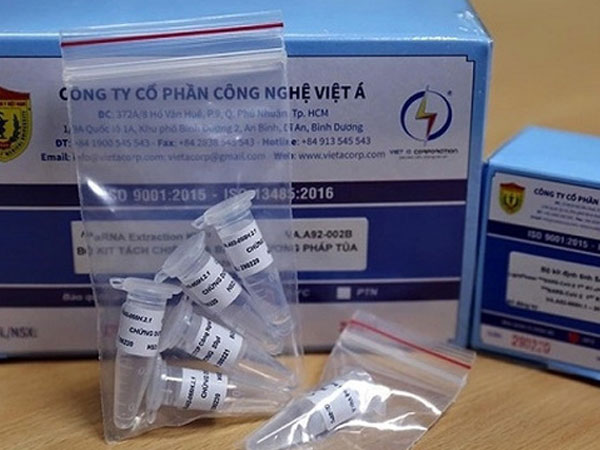
Trong bối cảnh dịch bệnh COVID-19 gần 2 năm qua, WHO đưa ra quy trình đánh giá sử dụng khẩn cấp (EUL) nhằm thúc đẩy sự sẵn có của các thiết bị y tế in vitro (trong ống nghiệm) cần cho các tình huống khẩn cấp về sức khỏe để hỗ trợ thông tin cho các cơ quan mua sắm và các nước thành viên Liên Hiệp Quốc.
Trang thiết bị y tế chẩn đoán in vitro được định nghĩa tại khoản 2, điều 2 nghị định 36/2016/NĐ-CP về quản lý trang thiết bị y tế là gồm thuốc thử, chất hiệu chuẩn, vật liệu kiểm soát, dụng cụ, máy, thiết bị hoặc hệ thống được sử dụng riêng rẽ hoặc kết hợp theo chỉ định của chủ sở hữu để phục vụ cho việc kiểm tra các mẫu vật có nguồn gốc từ cơ thể người.
Trên cơ sở đánh giá sử dụng khẩn cấp, các quốc gia có thể quyết định phê duyệt, sử dụng các sản phẩm cụ thể đã được chấp thuận trong bối cảnh khẩn cấp về y tế, dựa trên dữ liệu về chất lượng, an toàn và hiệu quả đã được thẩm định.
Quy trình EUL bao gồm đánh giá hệ thống quản lý chất lượng và kế hoạch giám sát sau thị trường của nhà sản xuất, đánh giá tài liệu cụ thể về sản xuất cũng như các bằng chứng về tính an toàn và hiệu quả.
WHO kết luận: bộ xét nghiệm LightPower iVASARS-CoV-2 1stRT-rPCR Kit với mã sản phẩm VA.A02-055H, sản xuất bởi Công ty cổ phần công nghệ Việt Á, địa chỉ 372A/8 Hồ Văn Huê, phường 9, quận Phú Nhuận, TP.HCM không đủ điều kiện để vào chương trình mua sắm của WHO.
Lần cập nhật ngày 9-6-2021, WHO tiếp tục công bố danh sách các sản phẩm không được chấp nhận theo quy trình đánh giá sử dụng khẩn cấp với lưu ý các hồ sơ đã được đánh giá và không cung cấp được bằng chứng, tài liệu cần thiết về an toàn, hiệu quả và/hoặc hệ thống quản lý chất lượng (QMS).
Trong danh sách này, ở mục xét nghiệm virus SARS‐CoV‐2, có tên bộ xét nghiệm LightPower iVASARS-CoV-2 1stRT-rPCR Kit, mã số sản phẩm VA.A02-055H, số hồ sơ đăng ký EUL 0524-210-00.
Có thể hiểu mã số EUL 0524-210-00 là mã số xác nhận khi công ty đăng ký thẩm định với WHO, không liên quan gì đến việc bộ xét nghiệm này được chính thức cấp phép theo các tiêu chí về an toàn và hiệu quả.

Nguyên nhân, theo WHO, VietACorp được yêu cầu cung cấp thông tin cập nhật về tình trạng của hệ thống quản lý chất lượng. Sau khi xem xét tài liệu được đệ trình, WHO hỗ trợ đánh giá về Hệ thống quản lý chất lượng của nhà sản xuất. Kết quả, thông tin được cung cấp không phải là bằng chứng đầy đủ về việc tuân thủ tiêu chuẩn ISO 13485:2016.
ISO 13458:2016 là tiêu chuẩn đã được chấp nhận và được áp dụng rộng rãi cho các nhà sản xuất thiết bị y tế trên toàn thế giới, và là một yêu cầu cần phải có nếu như một tổ chức sản xuất thiết bị y tế muốn sản phẩm của mình được công nhận rộng rãi trên thế giới. Phiên bản ISO 13458:2016 của WHO là “Hướng dẫn về Yêu cầu nộp hồ sơ: Chẩn đoán trong ống nghiệm (IVD) Phát hiện Axit nucleic SARS-CoV-2, PQDx_ 347”.
Bộ Y tế nói gì?
Về việc WHO không chấp nhận kit của VietACorp, thông tin từ Bộ Y tế chiều nay 20.12, cho biết: “WHO đưa ra danh sách EUL về một số sản phẩm để các đơn vị của WHO tham khảo và mua sắm khẩn cấp phục vụ phòng chống dịch, chứ không liên quan đến chất lượng hay tiêu chuẩn cấp phép”.
Theo Bộ Y tế, sản xuất trang thiết bị y tế trong nước, bao gồm kit test chẩn đoán từ ngày 1.1.2020, phải đạt tiêu chuẩn ISO 13485. Theo đó, VietACorp đã đạt tiêu chuẩn này khi sản xuất kit test xét nghiệm Covid-19.
Như vậy, có thể thấy, sản phẩm kit test của Công ty CP công nghệ Việt Á đạt tiêu chuẩn trong nước nhưng không đạt tiêu chuẩn và được WHO chấp nhận.
Trong khi đó, liên quan đến sản phẩm kit test này, vào thời điểm tháng 4.2020, có rất nhiều thông tin từ các cơ quan chức năng khẳng định WHO chấp thuận được sử dụng rộng rãi. Trong đó, trang web của Bộ KH-CN nhiều lần đưa tin WHO đã chấp nhận, tuy nhiên đến ngày 20-12, trên website của Bộ Khoa học và Công nghệ, thông tin công bố đánh giá của Tổ chức Y tế thế giới (WHO) và Bộ Y tế Anh cấp chứng nhận đạt chuẩn châu Âu cho bộ kit test của Công ty cổ phần Công nghệ Việt Á đã bị gỡ bỏ.
Ông Trịnh Thanh Hùng, Phó Vụ trưởng Vụ Khoa học và Công nghệ các khối ngành Kinh tế - Kỹ thuật, Bộ Khoa học và Công nghệ, thừa nhận Bộ đã chưa xem xét kỹ lưỡng thông tin phản hồi của WHO về bộ kit test của Công ty Việt Á.
"WHO mới chỉ "chấp thuận đưa kit test này vào quy trình đánh giá xem xét sử dụng" không phải "chấp thuận sử dụng". "Đây là sơ suất của Bộ Khoa học và Công nghệ"- ông nói.
Trước đó, ông Phan Quốc Việt (41 tuổi), Tổng giám đốc VietACorp, cùng nhiều thuộc cấp đã bị Bộ Công an khởi tố, điều tra về hành vi "thổi giá" kit xét nghiệm Covid-19.
VietACorp quảng cáo đây là bộ kit chẩn đoán SARS-CoV-2 đầu tiên tại Việt Nam, được Bộ Y tế cấp số đăng ký; Bộ Y tế và Chăm sóc xã hội Anh cấp giấy chứng nhận đạt tiêu chuẩn châu Âu (CE), cấp giấy chứng nhận lưu hành tự do (CFS); WHO cấp chứng nhận chất lượng sản phẩm cho phép lưu hành toàn cầu.
Cũng theo quảng bá, năng lực sản xuất của Công ty CP công nghệ Việt Á khoảng 30.000 kit xét nghiệm/ngày. Bộ kit xét nghiệm này cho kết quả chính xác 100% sau 2 giờ và đáp ứng được các tiêu chí tương đương các bộ sinh phẩm do CDC Mỹ và WHO hướng dẫn.
Ngọc Trâm (Nguoiduatin.vn)








- Tất cả người dân chú ý: Hàng triệu xe máy đối mặt với bộ quy chuẩn nghiêm ngặt từ cuối tháng 6 (22:00)
- Xiaomi Việt Nam chính thức lên tiếng sau khi nhận án phạt hành chính 290 triệu đồng (30 phút trước)
- Tổng thống Mỹ Donald Trump hé lộ ý định trực tiếp gặp Lãnh tụ Tối cao Iran (47 phút trước)
- Đón tín hiệu vui từ xăng E10: Dự báo giảm sâu gần 1.500 đồng/lít và hướng tới cơ chế giá độc lập (1 giờ trước)
- Xót xa vụ bé trai 11 tuổi tử vong nghi do mẹ kế bạo hành: Cả xóm ngỡ ngàng vì "chưa từng biết sự tồn tại của em" (1 giờ trước)
- Dự báo điểm chuẩn lớp 10 tại TP.HCM: Đề "dễ thở", sức nóng cạnh tranh tăng cao (1 giờ trước)
- Đào móng xây dựng khiến nhà hàng xóm nghiêng lún, hàng chục hộ dân phải sơ tán, chủ nhà lên tiếng (2 giờ trước)
- Bước ngoặt vụ nữ sinh bị sát hại "ngẫu nhiên" tại Hàn Quốc: Lật tẩy động cơ đê hèn của hung thủ (3 giờ trước)
- Chân dung nữ Chủ tịch CCV Group: Từ “để tôi vẽ hộ tương lai cho mọi người” đến lừa đảo nghìn tỷ (3 giờ trước)
- Hoa hậu Thùy Tiên có đủ điều kiện hưởng đặc xá năm 2026 hay không? (4 giờ trước)
Bài đọc nhiều